

发布时间:2020-07-19 14:48:57
原电池和电解池
1.原电池和电解池的比较:
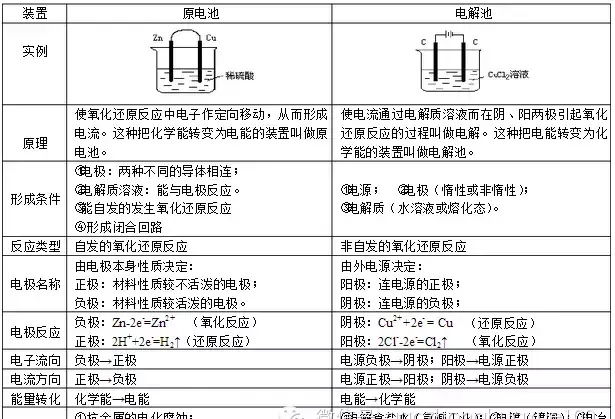
2原电池正负极的判断:
⑴根据电极材料判断:活泼性较强的金属为负极,活泼性较弱的或者非金属为正极。
⑵根据电子或者电流的流动方向:电子流向:负极→正极。电流方向:正极→负极。
⑶根据电极变化判断:氧化反应→负极; 还原反应→正极。
⑷根据现象判断:电极溶解→负极; 电极重量增加或者有气泡生成→正极。
⑸根据电解液内离子移动的方向判断:阴离子→移向负极;氧离子→移向正极。
3电极反应式的书写:

4.化学腐蚀和电化腐蚀的区别

5.吸氧腐蚀和析氢腐蚀的区别

考点解说
6.金属的防护
⑴改变金属的内部组织结构。合金钢中含有合金元素,使组织结构发生变化,耐腐蚀。如:不锈钢。⑵在金属表面覆盖保护层。常见方式有:涂油脂、油漆或覆盖搪瓷、塑料等;使表面生成致密氧化膜;在表面镀一层有自我保护作用的另一种金属。⑶电化学保护法 ①外加电源的阴极保护法:接上外加直流电源构成电解池,被保护的金属作阴极。②牺牲阳极的阴极保护法:外加负极材料,构成原电池,被保护的金属作正极
7. 常见实用电池的种类和特点

8.电解池的阴阳极判断:
⑴由外电源决定:阳极:连电源的正极; 阴极:连电源的负极;
⑵根据电极反应: 氧化反应→阳极 ;还原反应→阴极
⑶根据阴阳离子移动方向:阴离子移向→阳极;阳离子移向→阴极,
⑷根据电子几点流方向:
电子流向: 电源负极→阴极;阳极→电源正极
电流方向: 电源正极→阳极;阴极→电源负极
9.电解时电极产物判断:
⑴阳极:如果电极为活泼电极,Ag以前的,则电极失电子,被氧化被溶解,Zn-2e-=Zn2+
如果电极为惰性电极,C、Pt、Au、Ti等,则溶液中阴离子失电子,4OH-- 4e-= 2H2O+ O2 阴离子放电顺序S2->I->Br->Cl->OH->含氧酸根>F-
⑵阴极:(.阴极材料(金属或石墨)总是受到保护)根据电解质中阳离子活动顺序判断,阳离子得电子顺序 — 金属活动顺序表的反表金属活泼性越强,则对应阳离子的放电能力越弱,既得电子能力越弱。 K+ <Ca2+ < Na+ < Mg2+ < Al3+< (H+) < Zn2+ < Fe2+ < Sn2+ < Pb2+ < Cu2+ < Hg2+ < Ag+
10.电解、电离和电镀的区别

11.电镀铜、精炼铜比较
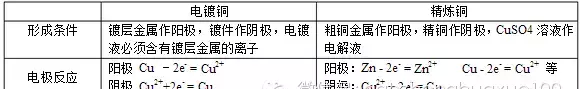
12.电解方程式的实例(用惰性电极电解):
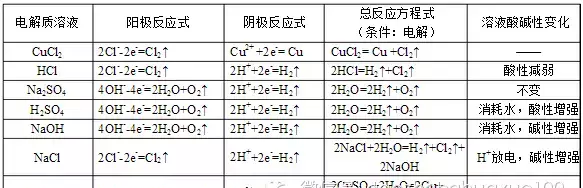
13,以惰性电极电解电解质溶液的规律:

14 . 电解原理的应用
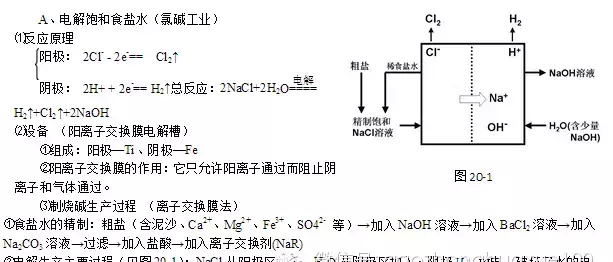

喜欢本篇文章,请随手点赞,欢迎分享到朋友圈
文章转自网络,因无法查询出处无法标注来源,如有侵权,请联系管理员删除。
➲老师的微信号:ziluolanzz
➲初中化学QQ:2506716372
➲初中化学微信:chuzhonghuaxue100
欢迎分享转载 →【史上最全】原电池和电解池 “知识点+考点”!